第五章 多原子分子结构与性质
 知识点三:多原子分子的振动光谱
知识点三:多原子分子的振动光谱
在前面内容中介绍了双原子分子的振动光谱,运用谐振子模型成功地讨论了振动光谱的起因和规律。其中最重要的结论为:一个确定的双原子分子对应用于一个确定的特征振动频率。这一结论与实验测得的振动光谱中存在一条最强的谱线相符。这给我们以启发,在讨论多原子分子的振动光谱时,是否一些具有特征的化学键在振动光谱中存在对应的强特征谱线呢? 实验证明确实如此。
一、分子振动的自由度
由于多原子分子振动的复杂性,常把分子的振动分为基本振动方式和复杂振动方式。复杂振动方式可视为基本振动方式的叠加。这是讨论复杂问题时常用的科学方法。基本振动方式又称为简正振动,是相互独立的振动方式。故简正振动的数目可由分子振动的自由度来确定。
若分子由n个原子组成,运动总自由度为3n。分子的平动用去3个自由度,转动占3个自由度(线性分子因绕轴转动时实际未动故为2)。这样分子有3n-6个振动自由度(线性分子为3n-5)。由此可知,双原子分子只有一种用谐振子模型描述的简正振动。
多原子分子的简正振动按振动方式可分为二类:一类是仅键长改变而键角不变,称为伸缩振动。另一类是仅键角改变而键长不变,称为弯曲振动。如前所述,分子的各种复杂振动可表示成有关简正振动的叠加。
H2O分子为非线性分子,振动自由度为3×3-6=3。考虑到两个O-H键是等价的,可有下面三种简正振动方式:
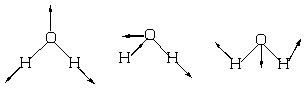
1 2 3
图5-4.1 水分子的三种简正振动
二、 分子的红外光谱及其应用
(1)水分子的红外光谱 振动光谱的选律告诉我们,只有在振动态的跃迁过程中分子偶极矩发生变化的振动才会出现红外光谱,此种振动被称为具有红外活性。H2O中的O-H键为极性键,三种简正振动都将引起分子偶极矩的变化故都具有红外活性。因不对称伸缩振动引起的偶极矩变化最大,故对应的谱线最强。而弯曲振动只引起分子键角的改变,能量和偶极矩变化的幅度较小,故对应的谱线波数应最小,也相对弱。图5-4.2 给出H2O分子的红外吸收谱,确实只有三个强吸收峰。根据上面的分析,可易指认最强且波数最大的吸收峰3.765×105m-1峰对应水分子的不对称伸缩振动,3.652×105m-1 峰对应对称伸缩振动,波数最小的1.595×105m-1 峰对应弯曲振动。

图5-4.2 水分子的红外光谱
(2)二氧化碳的红外光谱 CO2 是线性分子分子振动自由度为:3×3-5=4。图5-4.2给出 CO2 的四种简正振动方式。
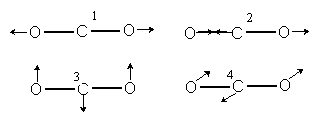
图5-4.3 CO2分子的四种简正振动
C-O键为极性键,但CO2 因其具有对称中心是非极性分子。故对称伸缩振动1因始终保持分子的中心对称为非红外活性,而反对称伸缩振动2和弯曲振动3、4破坏了分子的中心对称是红外活性的。二种弯曲振动能量是简并的对应一条谱线。CO2 的红外吸收谱,确实只有二个主吸收谱。依据以上分析,波数为2.349×105m-1 的强吸收峰可指认为对应分子的反对称伸缩振动,而波数为6.77×104m-1 的弱吸收峰对应分子的弯曲振动。
(3)红外光谱在分子结构测定中的应用 通过对大量多原子分子的振动光谱分析后发现,若不同分子含有相同的化学基团时,如-C≡N、-CH3、-O-H,则在这些分子光谱中常有频率相同或相近的谱线出现。因此在红外光谱中,把能代表某种化学基团存在的最强峰称为该基团的特征峰,对应的频率称为该基团的特征频率。
现已有不少红外光谱的工具书详细收录了多种基团特征频率出现的范围,并讨论了影响其强度的因素。这使红外光谱成为表征样品的分子结构的十分有力的实验手段。表5-4.1列出一些常见化学基团振动吸收频率的范围。
红外光谱按波段及其对应的化学键可分为四个区:
4000~2500×102m-1的高频区,为含氢化学键的伸缩振动区。这是由氢原了质量最小造成的。
2500~2000×102m-1是三重键的振动区,因为三重键的力常数十分大。
2000~1600×102m-1为双重键的振动区。
以上三个区为基团频率区或特征频率区,可用于鉴定测试样品里所含的官能团。
最后一区为1600~500×102m-1,对应单键的伸缩和弯曲振动。这个区域图谱复杂,并对结构上的微小变化非常敏感。分子只要在化学结构上存在细小的差异,如同系物、同分异构体和在空间构象上存在差异,在这一区域的谱线情况都将发生明显变化,如同人的指纹一样。故该区被称为指纹区,其价值在于它可表示整个分子的特征,对检定化合物是很有用的。
红外光谱的解释在许多情况下往往还需经验的帮助。这是因为化学键的频率与周围的化学环境存在相当敏感的依赖关系。
表5-4.1 红外光谱中一些基团的吸收区域(102m-1)
![]()
![]()
基团 吸收频率 振动形式 吸收强度
![]()
-OH(游离) 3650~3580 伸缩 中
-OH(缔合) 3400~3200 伸缩 强
-NH2(游离) 3500~3300 伸缩 中
-NH(缔合) 3400~3100 伸缩 强
≡C-H ~3300 伸缩 强
=C-H 3010~3040 伸缩 强
苯环中C-H ~3030 伸缩 强
-CH3 2960± 5 反对称伸缩 强
2870±10 对称伸缩 强
-CH2 2930±5 反对称伸缩 强
2850±10 对称伸缩 强
-S-H 2600~2500 伸缩 强
-C≡N 2260~2220 伸缩 强
-N≡N 2310~2135 伸缩 中
R-C≡C-R 2260~2100 伸缩 随R、R′变化
C=C 1680~1620 伸缩 中、弱
芳环中C=C 1600,1580 伸缩 可变
1500,1450
-C=O 1850~1600 伸缩 强
-NO2 1600~1500 反对称伸缩 强
1300~1250 对称伸缩 强
C-O 1300~1000 伸缩 强
C-O-C 900~1150 伸缩 强
C-F 1400~1000 伸缩 强
C-Cl 800~600 伸缩 强
C-Br 600~500 伸缩 强
C-I 500~200 伸缩 强
![]()
(4)喇曼(Raman)光谱 红外光谱研究的是分子因吸收或发射一个光子而引起振动—转动能级跃迁的过程。还有另一种研究分子振动—转动能级状态的方法,叫喇曼光谱。与红外光谱不同,喇曼光谱研究的是被样品散射的光。
当光子与分子碰撞时,若光子的能量正好与分子的二个能级差相等时,分子可吸收光子跃迁到高能级。在许多情况下,分子也可散射光子。在这种散射光中,绝大部分光频率未变(称为弹性散射),只有极少量光频率略有变化(称为非弹性散射)。有关的量子力学研究指出,在非弹性散射过程中光子能量的改变值应等于被碰撞分子在两能级间的跃迁能。喇曼光谱正是通过对这种非弹性散射光的测量,去获取样品分子振动—转动能级状态的有关信息。但由于非弹性散射光只有入射光强度的10-6,当入射光为普通光时,喇曼光谱很难观测。当用光强极强的激光做光源时,喇曼光谱才进入实用阶段。故现在实用的是激光喇曼光谱。
喇曼光谱的选律为样品分子应具有各向异性的极化率。对于同核双原子分子,例如H2分子,因其具有对称中心使其振动和转动跃迁为非红外活性。但这些分子沿键轴方向的极化率与垂直于键轴方向的极化率存在明显差别,它们的振动和转动能级跃迁都为喇曼活性。这样喇曼光谱和红外光谱在研究样品分子时相互补充,使研究更深入和全面。由于喇曼光谱研究的是非弹性散射光,其入射的激光通常为紫外可见光,这样相当于把样品分子的振动—转动能级从红外区移到紫外可见区来研究。
例:乙炔为线性分子,振动自由度为4×3-5=7。
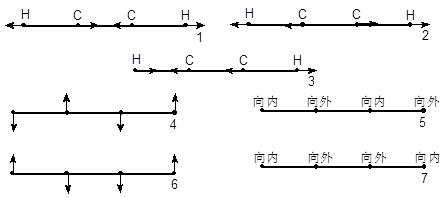
图5-4.4 乙炔的7种简正振动
乙炔具有对称中心,为线性共轭结构,极化率各向异性。1、2、4、5振动保持分子中心对称,具有喇曼活性(4、5为二重简并)。3、6、7振动因破坏了分子中心对称,发生极性变化,具有红外活性(6、7二重简并)。
