当前位置:课程学习>>第六章>>知识讲解>>视频课堂>>知识点一
知识点一:配位场理论简介
同学们,请运用你学到的知识,尝试分析下面的问题。
问题:已知[Fe(H2O)6]3+的分裂能为13700 cm-1若Fe3+的成对能分别为19150cm-1,试用稳定化能判断d电子构型和未成对电子数。
教师解析
[Fe(H2O)6]3+中的Fe3+为d5组态,d电子有两种排布方式,第一种为低自旋排布(t2g)5(eg)0,晶体场稳定化能为:
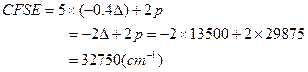
另一种为高自旋排布(t2g)3(eg)2,晶体场稳定化能为:
![]()
[Fe(H2O)6]3+中有d电子 排布为(t2g)3(eg)2,未成对电子数量是5。
掌握了这个问题的答案,可以为后面的学习奠定基础。
通过对上述问题的分析,你是否掌握了理论知识?下面我们进入总结与反思。
