当前位置:课程学习>>第一章 热力学第一定律>>知识讲解>>视频课堂>>知识点五
知识点五:热力学第一定律对理想气体的应用
理想气体的热力学能和焓
1843年焦耳(Joule)设计了如下实验:
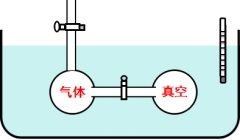
打开活塞后,作自由膨胀,W=0;水温未变,Q=0;∆U=Q+W=0。
结论:气体经自由膨胀热力学能不变。
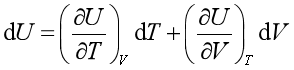
因dT=0, dU=0,则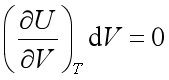
因dV>0,则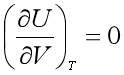
同理可证: 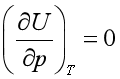
说明气体的热力学能U只是温度的函数,而与体积和压力无关。事实上,上面实验不够精密,但其结论只适用于理想气体。U=f(T)
对理想气体,pV=nRT,则
H=U+nRT
即H=g(T),理想气体的焓也只是温度的函数。对理想气体的任何过程:
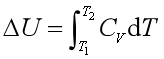
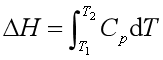
接下来让我们进行下一部分的学习
