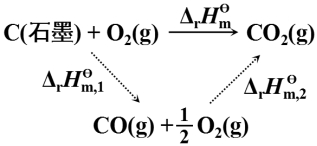当前位置:课程学习>>第一章 热力学第一定律>>知识讲解>>视频课堂>>知识点七
知识点七:热化学
一、定压热![]() 与定容热
与定容热![]() 的关系
的关系
热力学函数的变化![]() (或
(或![]() )的测定来源于量热实验,依据于
)的测定来源于量热实验,依据于![]() =
=![]() ,
,![]() =
=![]() 两式,
两式,![]() 和
和![]() 的测量条件不同,可进行如下换算:
的测量条件不同,可进行如下换算:
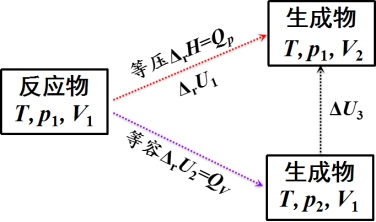
![]() =
=![]() +
+![]() (V2-V1)
(V2-V1)
![]() =
=![]() +
+![]()
![]()
![]()
![]() =
=![]() +
+![]() (V2-V1) =
(V2-V1) =![]() +
+![]()
![]()
(1)对凝聚系统的反应,![]()
(2)对理想气体反应,![]()
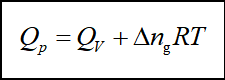
对复相反应,上式仍适用。式中![]() 。
。
二、盖斯(Hess)定律
1836年盖斯:“一个化学反应,不论是一步完成,还是分几步完成,其标准摩尔焓变总是相同的。”
例:![]()
![]()
![]()
![]()
![]()
![]()
盖斯定律是热力学第一定律应用于化学反应的必然结果。其意义在于,利用热化学方程式的线性组合,可由已知反应的![]() 求得实验上难于测量的反应的
求得实验上难于测量的反应的![]() 。例如:
。例如: