一、填空题
1、偏微商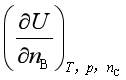 的名称叫 ;偏微商
的名称叫 ;偏微商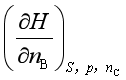 的名称叫 。
的名称叫 。
2、偏摩尔体积的定义式为![]() ;化学势的定义式为
;化学势的定义式为![]() ;
;
3、理想气体混合物中任一组分B的化学势为![]() 0,式中
0,式中![]() 是组分B在 状态时的化学势。
是组分B在 状态时的化学势。
4、纯实际气体的化学势表示为![]()
![]() ,式中
,式中![]() 称为实际气体的 。
称为实际气体的 。
5、按定义: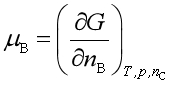 ,
,![]() 称为 ,也称为 。
称为 ,也称为 。
6、理想液态混合物中任一组分B的化学势![]() +
+![]() 。
。
7、在温度和物质组成不变的条件下,组分B的化学势![]() 随压力
随压力![]() 的变化率
的变化率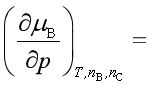 。在压力和物质组成不变的条件下,组分B的化学势
。在压力和物质组成不变的条件下,组分B的化学势![]() 随温度
随温度![]() 的变化率
的变化率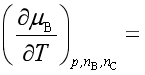 。
。
8、已知水(A)和乙醇(B)的物质的量分别为![]() 和
和![]() ,水和乙醇的偏摩尔体积分别为
,水和乙醇的偏摩尔体积分别为![]() 和
和![]() ,则乙醇水溶液的总体积
,则乙醇水溶液的总体积![]() 。水和乙醇偏摩尔体积所遵从的吉布斯—杜亥姆公式为: 。
。水和乙醇偏摩尔体积所遵从的吉布斯—杜亥姆公式为: 。
9、拉乌尔定律的数学表达式为![]() ;亨利定律的数学表达式为
;亨利定律的数学表达式为![]() 。
。
10、理想稀溶液中的 服从拉乌尔定律, 服从亨利定律。
二、判断题(对者写“√”,错者写“×”)
1、1升乙醇和1升水混合后,其体积刚好等于2升。
2、溶液的化学势等于溶液中各组分化学势之和。
3、理想稀溶液中溶剂分子与溶质分子之间只有非常小的作用力,以至可以忽略不计。
4、系统处于平衡状态时,偏摩尔量为一个确定的值。
5、对于纯物质而言,化学势等于其摩尔吉布斯自由能。
6、将少量乙醇溶于水中形成稀溶液,则该溶液的沸点和凝固点均低于纯水。
7、理想液态混合物中各种组分之间的相互作用可以忽略不计。
8、对理想液态混合物中的组分而言,亨利定律和拉乌尔定律具有相同的形式。
9、溶质溶于溶剂形成溶液,当溶质用不同的浓度表示时,则溶质化学势的数据都相同。
10、水溶液的蒸气压一定小于同温度下纯水的饱和蒸气压。
三、单项选择题(下列各题的4个选项中,只有1个正确答案)
1、下列各式表示的是偏摩尔量
A、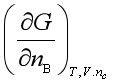 B、
B、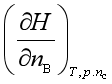 C、
C、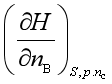 D、
D、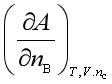
2、下列各式哪个是化学势
A、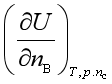 B、
B、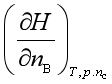 C、
C、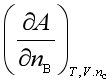 D、
D、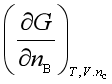
3、在298.2 K、101325 Pa压力下,两瓶体积均为1 dm3萘溶于苯的稀溶液,第1瓶中含萘1 mol;第2瓶中含萘0.5 mol。若以![]() 及
及![]() 分别表示两瓶萘的化学势,则
分别表示两瓶萘的化学势,则
A、![]() >
>![]() B、
B、![]() <
<![]() C、
C、![]() =
=![]() D、不能确定
D、不能确定
4、5℃时,A与B两种气体的亨利系数关系为kA > kB,将A与B同时溶解在某溶剂中达到溶解平衡,若气相中A与B的平衡分压相同,那么溶液中的A、B的浓度为:
A、mA < mB B、mA > mB C、mA = mB D、无法确定
5、下列气体溶于水溶剂中,哪个气体不能用亨利定律
A、N2 B、O2 C、NO2 D、CO
6、在恒温密封容器中有A、B两杯稀盐水溶液,盐的浓度分别为cA和cB,且cA > cB,放置足够长的时间后
A、A杯盐的浓度降低,B杯盐的浓度增加
B、A杯液体量减少,B杯液体量增加
C、A杯盐的浓度增加,B杯盐的浓度降低
D、A、B两杯中盐的浓度会同时增大
7、298 K、101.325 kPa下,将50 ml与100 ml浓度均为1 mol·dm-3 萘的苯溶液混合,混合液中萘的化学势![]() 为:
为:
A、![]() B、
B、![]()
C、![]() D、
D、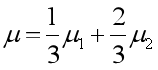
8、任一单组分系统,恒温下,其气(g)、液(l)态的化学势(μ)与压力(p)关系图正确是
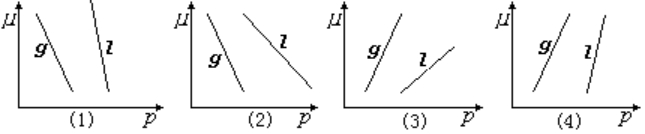
A、(1) B、(2) C、(3) D、(4)
9、苯(A)与甲苯(B)形成理想液态混合物,当把5 mol苯与5 mol甲苯混合时,与混合物相平衡的蒸气中,苯(A)的摩尔分数是
A、yA = 0.5 B、yA < 0.5 C、yA > 0.5 D、无法确定
10、关于二组分理想液态混合物的沸点的论述正确的是
A、沸点与混合物的组成无关 B、沸点在两纯组分的沸点之间
C、小于任一纯 组分的沸点 D、大于任一纯组分的沸点

