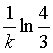一、填空题
1、在恒容条件下,反应速率![]() 的定义式为:
的定义式为:![]() 。对于基元反应:
。对于基元反应:![]() ,反应速率表示为:
,反应速率表示为:![]()
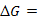 。
。
2、对于理想气体反应![]() ,反应速率方程有两种表示法:
,反应速率方程有两种表示法: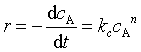 或
或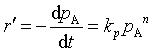 。则
。则![]()
![]() ;
;![]()
![]() 。
。
3、设反应![]() 为一级反应,则以 对反应时间
为一级反应,则以 对反应时间![]() 作图得一直线,该直线的斜率为 。
作图得一直线,该直线的斜率为 。
4、设反应![]() 为二级反应,则以 对反应时间
为二级反应,则以 对反应时间![]() 作图得一直线,该直线的斜率为 。
作图得一直线,该直线的斜率为 。
5、阿伦尼乌斯活化能Ea是 的平均能量与 平均能量之差。
6、在平行反应A![]() B,A
B,A![]() C中,Ea值 的反应,其反应速率大;升温对Ea值 的反应速率影响更大。
C中,Ea值 的反应,其反应速率大;升温对Ea值 的反应速率影响更大。
7、某反应进行时,反应物浓度与时间成线性关系,则该反应为 级反应,其半衰期![]() 与反应起始浓度
与反应起始浓度![]() 的关系是 。
的关系是 。
8、根据阿伦尼乌斯公式,以![]() 对 作图可得一条直线,直线的斜率为 。
对 作图可得一条直线,直线的斜率为 。
9、根据拟定的反应机理,推导总反应的速率方程时,可采取一定的近似方法,其中包括速率控制步骤(速控步)、 近似和 假设三种方法。
10、某一基元反应在指定温度下,当活化焓越 ,反应速率越快;当活化熵越 ,反应速率越快。
二、判断题(对者写“√”,错者写“×”)
1、零级反应一定不是基元反应。
2、若化学反应由一系列基元反应组成,则总反应的速率是各基元反应速率的代数和。
3、双分子反应一定是二级反应。
4、对于反应 A →产物,如果使A的起始浓度减小一半,其半衰期便缩短一半,则反应级数为零级。
5、一个化学反应进行完全所需的时间是半衰期的2倍。
6、基元反应:![]() 的活化能
的活化能![]() 等于键能
等于键能![]() 。
。
7、若某化学反应的![]() < 0,则该化学反应的活化能小于零。
< 0,则该化学反应的活化能小于零。
8、复合反应的总反应速率取决于其中最慢的一步。
9、有催化剂参加的反应(即催化反应)一定不是基元反应。
10、一个基元反应的逆向反应一定是基元反应。
三、单项选择题
1、在一定温度下,反应A+ B →2D的反应速率可表示为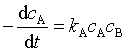 ,也可以表示为
,也可以表示为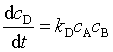 ,则速率系数kA 和kD 的关系为
,则速率系数kA 和kD 的关系为
A、kA =kD B、2kA = kD C、kA =2kD D、没有关系
2、温度T时,某理想气体反应的速率方程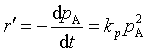 ,pA是为反应物的分压力,若将速率方程表示为
,pA是为反应物的分压力,若将速率方程表示为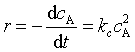 ,则下列关系正确的是
,则下列关系正确的是
A、![]() ,
,![]() B、
B、![]() ,
,![]()
C、![]() ,
,![]() D、
D、![]() ,
,![]()
3、均相反应 A + 2D → 3G 在298 K及1 dm3的容器中进行,若某时刻反应进度随时间变化率为 0.30 ![]() ,则此时G的生成速率为(单位:
,则此时G的生成速率为(单位:![]() )
)
A、0.10 B、0.90 C、0.15 D、0.20
4、某气相反应在动力学研究中表现为二级,则下面的说法中正确的是
A、它一定是双分子反应 B、它有可能是单分子反应
C、它不可能是复合反应 D、它不是双分子反应,就是复合反应
5、反应 A→B,实验测得A的浓度与时间t成直线关系,则反应为
A、1级 B、2级 C、分数级 D、零级
6、某反应进行完全所需时间是有限的,且等于![]() ,则该反应是
,则该反应是
A、零级反应 B、一级反应 C、二级反应 D、三级反应
7、某反应物当其浓度消耗![]() 所需的时间是它消耗
所需的时间是它消耗![]() 所需时间的2倍,则该反应级数为
所需时间的2倍,则该反应级数为
A、3 B、2 C、1 D、0
8、有关基元反应的描述,下列说法错误的是
A、基元反应的级数一定是整数 B、基元反应的活化能称为表观活化能
C、基元反应进行时无中间产物,一步完成 D、基元反应一定符合质量作用定律
9、净重为8 g的某物质的分解反应为一级反应,其半衰期为10天,则40天后其净重为
A、4 g B、2 g C、1 g D、0.5 g
10、已知A→B + C是基元反应,则反应物A消耗掉1/4所需的时间是
A、![]() B、
B、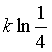 C、
C、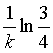 D、
D、