知识点二:电解时的电极反应
一、金属的析出与氢超电势
电解金属盐类(MX)的水溶液时,Mz+和H+析出的顺序决定于它们的析出电势。
【例题】298.2K时,用锌电极作阴极电解![]() 的ZnSO4水溶液。若在某一电流密度下氢气在锌电极上的超电势为0.7 V,问在常压下阴极析出的物质是氢气还是金属锌?
的ZnSO4水溶液。若在某一电流密度下氢气在锌电极上的超电势为0.7 V,问在常压下阴极析出的物质是氢气还是金属锌?
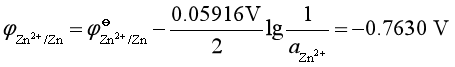
解:![]()
![]()
![]()
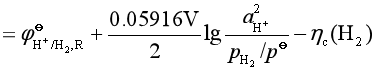
结论:若不考虑 ![]() ,H2先析出。当考虑
,H2先析出。当考虑![]() 时,
时,![]() 先析出。
先析出。
【思考题】试讨论金属活动顺序表。
二、金属离子的分离
若溶液中含有多种金属离子,可利用它们析出电势的不同进行分离。
例如,对![]() 和
和![]() 的混合溶液。若忽略金属析出的超电势,其析出电势分别为:
的混合溶液。若忽略金属析出的超电势,其析出电势分别为:
![]()
![]()
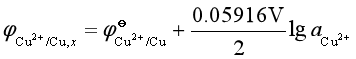
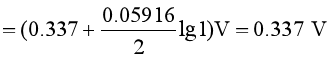
所以![]() 在阴极先析出。当
在阴极先析出。当![]() 时,可认为
时,可认为![]() 全部沉积,则此时
全部沉积,则此时
![]()
![]() 仍不能析出,其析出时
仍不能析出,其析出时
![]()
![]()
对金属离子的分离:达到![]()
一价金属离子:![]()
二价金属离子:![]()
三、金属离子的共同析出
设溶液中有![]() 和
和![]() 两种离子:
两种离子:

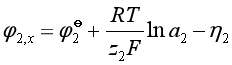
共同析出的条件是:
![]()
即 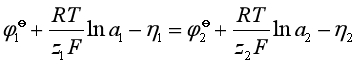
(1)对![]() 相差不大的情况。调整浓度:
相差不大的情况。调整浓度:
例如,![]() ,
,![]() ,当
,当![]() 时使它们共同析出。
时使它们共同析出。
(2)对 ![]() 相差较大的情况。改变配方:
相差较大的情况。改变配方:
例如:![]() ,
,![]()
加入![]() ,生成
,生成![]() 、
、![]() 络合离子,则
络合离子,则
![]() ,
,![]()
当电流密度![]() 时,
时,![]() ,
,![]() ,可计算出:
,可计算出:
![]()
![]()
进一步调整浓度:
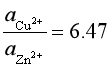
便可得到黄铜合金,这就是电镀工艺中合金电镀的基本原理。
接下来让我们进行下一部分的学习
