第九章 不可逆电极过程
 知识点二:电解时的电极反应
知识点二:电解时的电极反应
当电解池的外加电压由小到大逐渐变化时,可以造成电解池阳极电势逐渐升高、阴极电势逐渐降低。从整个电解池来说,只要外加电压达到分解电压![]() 的数值时,电解即进行;从各个电极的角度来说,只要电极电势达到对应离子的析出电势,则电解的电极反应即进行。
的数值时,电解即进行;从各个电极的角度来说,只要电极电势达到对应离子的析出电势,则电解的电极反应即进行。
一、金属的析出与氢超电势
当电解金属盐类(MA)的水溶液时,溶液中的阳离子M+和H+均趋向阴极,究竟何者先在阴极上析出?结论是极化(还原)电极电势愈正者,其氧化态优先还原而析出。
例1 298K时,用锌电极作为阴极电解![]() =1的ZnSO4水溶液。若在某一电流密度下氢气在锌极上的超电势为0.7V。问在常压下电解时,阴极上析出的物质是氢气还是金属锌?
=1的ZnSO4水溶液。若在某一电流密度下氢气在锌极上的超电势为0.7V。问在常压下电解时,阴极上析出的物质是氢气还是金属锌?
解: 锌在阴极上的超电势可以忽略,查表得![]() =-0.7630V。因
=-0.7630V。因![]() =1,故
=1,故
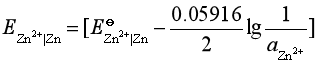 V = -0.7630V
V = -0.7630V
氢气在阴极上析出时的平衡电势(电极符号下角标![]() 表示平衡电势)
表示平衡电势)
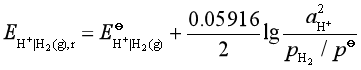
电解在常压下进行,氢气析出时应有![]() =101.325kPa,水溶液可近似认为中性, 并假定
=101.325kPa,水溶液可近似认为中性, 并假定![]() =10-7,于是
=10-7,于是
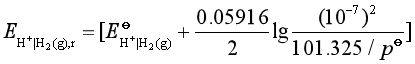 V = -0.4141V
V = -0.4141V
考虑到氢气在锌电极上的超电势![]() =0.7V,故析氢时的极化电极电势(下标
=0.7V,故析氢时的极化电极电势(下标![]() 表示析出电势)
表示析出电势)
![]() =-1.114V
=-1.114V
可见,若不存在氢的超电势,因![]() 比
比![]() 更正,应当在阴极上析出氢气;而由于氢超电势的存在,
更正,应当在阴极上析出氢气;而由于氢超电势的存在,![]() 比
比![]() 更正,故实际是Zn优先在阴极上析出。
更正,故实际是Zn优先在阴极上析出。
以上分析,未考虑浓差极化,这可以通过搅拌使之降至忽略不计。
一般说来,电解时,一方面应该注意因电解池中溶液浓度的改变所引起的反电动势的改变,同时还要注意控制外加电压不宜过大,以防止氢气也在阴极同时析出。
二、金属离子的分离
若溶液中含有多种金属离子,可利用金属析出电势的不同将它们分离。![]() 越正的离子,越易获得电子而还原成金属,电解时,阴极电势在由高变低的过程中,各种离子按其对应的
越正的离子,越易获得电子而还原成金属,电解时,阴极电势在由高变低的过程中,各种离子按其对应的![]() 由高到低的次序而先后析出。
由高到低的次序而先后析出。
例如,有一含0.01mol·dm-3的Ag+和1 mol·dm-3的Cu2+的硝酸盐溶液,其中![]() = 1 mol·dm-3,如忽略金属析出的超电势,则两种离子开始时的析出电势分别为
= 1 mol·dm-3,如忽略金属析出的超电势,则两种离子开始时的析出电势分别为
![]()
=(0.7991+0.05916lg0.01)V=0.681V
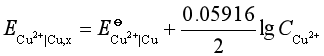
=(0.337+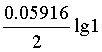 )V=0.337V
)V=0.337V
因![]() >
>![]() ,所以当阴极电势达0.681V时,Ag优先在阴极开始析出,假定溶液中的
,所以当阴极电势达0.681V时,Ag优先在阴极开始析出,假定溶液中的![]() =10-7 mol·dm-3时认为Ag+已全部沉积,则此时
=10-7 mol·dm-3时认为Ag+已全部沉积,则此时
![]() (0.7991+0.05916lg10-7)V = 0.385V
(0.7991+0.05916lg10-7)V = 0.385V
而Cu2+开始析出的电势是0.337V,因此,只要控制阴极电势在0.337V以上,则只会是Ag析出,从而实现将此溶液中的Ag+与Cu2+的分离。此时,可将阴极取出称量其电解前后的净增值即为析出Ag的量。然后,再插入另一新的电极,继续增加外电压,可使Cu2+沉积。
通常,电流密度较小时,金属离子析出超电势可以忽略,这样,就可用能斯特方程作一些离子分离的估算。例如,298K时,对一价金属离子,其浓度从1 mol·dm-3降至10-7 mol·dm-3时,![]() =0.41V。所以,要使两种一价金属离子电解分离,两者的电极电势要相差0.41V以上;同理,要使两种二价金属离子电解分离,两者的电极电势要相差0.21V以上。
=0.41V。所以,要使两种一价金属离子电解分离,两者的电极电势要相差0.41V以上;同理,要使两种二价金属离子电解分离,两者的电极电势要相差0.21V以上。
三、金属离子的共同析出
工业电镀常采用二元合金电镀,以获得具有特殊性能的镀层。例如黄铜(Cu-Zn合金)、青铜(Cu-Sn合金)、Pb-Sn合金和 Zn-Ni合金等。这都涉及到二种金属一起沉积的问题。
设溶液中有![]() 和
和![]() 两种离子,活度各为
两种离子,活度各为![]() 1和
1和![]() 2。由能斯特方程:
2。由能斯特方程:
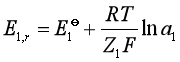 (13)
(13)
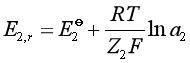 (14)
(14)
显然,在可逆还原过程中,两种离子同时在电极上沉积的可能性是
![]()
但若![]() 比
比![]() 更正,则M1当在M2之前析出,且
更正,则M1当在M2之前析出,且![]() 和
和![]() 差距越大,M2的析出电势就离M1越远。实际电解时,离子的沉积电势必定偏离平衡值,但不管怎样,两种离子同时析出的前提总是
差距越大,M2的析出电势就离M1越远。实际电解时,离子的沉积电势必定偏离平衡值,但不管怎样,两种离子同时析出的前提总是
![]() =
=![]()
若M1和M2的超电势分别为:
![]() 及
及![]()
则得 ![]()
或进一步写为:
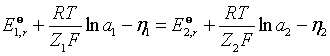 (15)
(15)
从上式可见,适当选择![]() ,
,![]() 和
和![]() 值,就能使两种离子共同析出。一般,金属沉积时,超电势都不大,故共沉积或先后析出的次序可大体参考标准电极粗略估计。例如,铅和锡,
值,就能使两种离子共同析出。一般,金属沉积时,超电势都不大,故共沉积或先后析出的次序可大体参考标准电极粗略估计。例如,铅和锡,![]() =-0.126V,
=-0.126V,![]() =-0.136V。两者相当接近,且
=-0.136V。两者相当接近,且![]() 又都甚小。于是,只要适当调节组分的浓度比,便可以使它们一起沉积出来。但对于锌和铜,
又都甚小。于是,只要适当调节组分的浓度比,便可以使它们一起沉积出来。但对于锌和铜,![]() =-0.763V,
=-0.763V,![]() =0.337V,则因
=0.337V,则因![]() 值相差甚远,在它们的简单盐溶液中,即使Cu2+沉积殆尽也不会有Zn2+开始析出。然而,倘能改换配方,比如,用它们的配合氰化物配成混合溶液。即在溶液中加入CN-离子(加NaCN),由于生成了配合离子Cu(CN)3-,
值相差甚远,在它们的简单盐溶液中,即使Cu2+沉积殆尽也不会有Zn2+开始析出。然而,倘能改换配方,比如,用它们的配合氰化物配成混合溶液。即在溶液中加入CN-离子(加NaCN),由于生成了配合离子Cu(CN)3-,![]() ,使得
,使得![]() =-0.763V,
=-0.763V,![]() =-1.108V,两者仅差0.345V,再考虑两者的超电势不同,例如当阴极电流密度
=-1.108V,两者仅差0.345V,再考虑两者的超电势不同,例如当阴极电流密度![]() =0.005A·cm-2时,
=0.005A·cm-2时,![]() =0.685V,
=0.685V,![]() =0.316V,可计算出
=0.316V,可计算出
![]() = -1.448V
= -1.448V
![]() =-1.424V
=-1.424V
两者只差0.024V,如果进一步通过调节温度、电流密度、氰根(CN-)离子浓度,就可以电解沉积得到黄铜合金。这就是电镀工艺中合金电镀的基本原理,可以用以解决实际问题。
