|
(一)实验操作
1、溶液配制
用称量法配制四个25毫升浓度为 C4H6O2(乙酸乙酯)-CCl4(四氯化碳)溶液,分别盛于容量瓶中,其浓度(摩尔分数)分别为0.010、0.050、0.100、0.150左右。操作时应注意防止溶质、溶剂的挥发以及吸收极性较大的水气,为此溶液配好后应迅速盖上瓶塞。
2、折射率测定
用阿贝折射仪测定四氯化碳及配制各溶液的折射率。阿贝折射仪的使用。
3、介电常数测定
介电常数是借助于小电容测试仪通过测定电容计算而得的。PGM-Ⅱ型数字小电容测试仪能进行电容量的测定,而且可和电容池配套对溶液和溶溶剂的介电常数进行测定。如果在电容器的两个极板间充以某种电解质,电容器的电量就会增大。如果维持极板上的电荷量不变,那么充以电解质的电容器二极板间电势差就会减少。设C0为极板间处于真空时的电容量,C为充以电解质时的电容量,则C与C0之比值ε称为该电解质的介电常数:
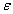 = = 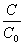
在实验中采CCl4为标准物质,其介电常数的温度公式为:
εCCl4=2.238-0.0020(t-20)
式中的t为室温温度(摄氏温标)。
(二)数据记录与处理
1.计算各溶液的摩尔分数浓度X1, X2。
2.计算各溶液的Y和C2值,作Y--- C2图,由直线斜率求算B值。
3.将B值代入公式计算四氯化碳的永久偶极矩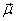 值。 值。
|