【实验关键提示】
1. 利用惠斯登电桥测定溶液的电导,关键是找到电桥的平衡点,一般测量步骤是,先选择R2/R1=1(理论上讲,此时所得到的结果的误差最小),再调节R3使通过示波器H的信号最小。但在测量电导水时,由于Rx较大,可选择R2/R1=10或R2/R1=100。
2. 对交流信号来说,电导池Rx的两个电极相当于一个电容器,这一结果使电桥两支线的位相不同,因而找不到示波器H中信号完全消失的位置,对于精确的测量,需要在电阻R3上并联一个可变电容器C1,以实现容抗平衡。另外,为避免外来电磁波的干扰,最好使用屏蔽导线,接线柱的裸露部分尽量缩短。
3. 由于温度变化会影响电导,一般在室温下温度升高1oC,电导将增加2%,因此测量时应注意保持恒温,待测液一般需恒温10 min。
4. 本实验所测定的醋酸溶液及电导水的电导率都是很小的,若其中有微量的杂质会引起很大的实验误差,因此实验过程中必须保持样品的纯度,石英蒸馏器制备的二次蒸馏水的电导率应小于1×10-4 S・m-1,测量样品的步骤遵循电导率由小到大的先后顺序,测量时电导池和电导电极要用待测液洗干净。
5.本实验所用电导电极是镀铂黑的铂电极,镀铂黑的目的是为了增大电极的表面积,减小电流密度,从而降低由电流引起的极化效应,因此在实验过程中不要用滤纸擦拭铂黑,以免使铂黑脱落而改变电导池系数。实验结束后,用蒸馏水冲洗电极,最后浸泡在蒸馏水中。
【讨论】
电导测定不仅有助于研究电解质溶液的特性,也可直接用来解决一些化学问题,诸如计算水的离子积,难溶盐的溶解度和弱电解质的解离度等。对于这些浓度极低的体系,一般的分析方法难以精确测定。然而,正是由于浓度低,离子间的相互作用可以忽略,才有
Λm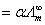 一式成立,这便为电导法解决问题提供了方便。根据 一式成立,这便为电导法解决问题提供了方便。根据 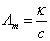 可得: 可得:
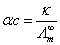
对于强电解质(如AgCl、PbSO4等)溶液,α=1,通过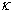 和 和 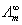 可以计算出其溶解度c;对于弱电解质(如HAc等),通过 可以计算出其溶解度c;对于弱电解质(如HAc等),通过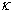 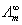 和c可以计算出解离度α。其中 和c可以计算出解离度α。其中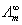 可以查表得到,因此电导法解决这类问题最终归结为电导率 可以查表得到,因此电导法解决这类问题最终归结为电导率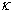 的精确测定。 的精确测定。
电解质溶液属于离子导体,其电阻同电子导体(如金属、石墨等)一样,也服从欧姆定律和
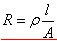 (推导)式,因此两者测量电阻的原理和方法相同,即可以利用惠斯登电桥。所不同的是,电解质溶液的导电机理是由正、负离子共同承担的,导电过程中在两电极上总是伴随着电化学反应,这种特殊性导致在测量技术上需做如下三点改变:(1)使用交流电源;(2)因采用交流电源,所以不能用直流检流器,而改用示波器或耳机;(3)需补偿电导池的电容。 (推导)式,因此两者测量电阻的原理和方法相同,即可以利用惠斯登电桥。所不同的是,电解质溶液的导电机理是由正、负离子共同承担的,导电过程中在两电极上总是伴随着电化学反应,这种特殊性导致在测量技术上需做如下三点改变:(1)使用交流电源;(2)因采用交流电源,所以不能用直流检流器,而改用示波器或耳机;(3)需补偿电导池的电容。
为防止电导池中溶液浓度改变而产生极化,交流电源的频率应高一些。但是另一方面,由于电阻箱(R1,R2,R3)存在电感和电容,电导池也有电容,因此在使用高频交流信号时,电桥平衡条件应当是: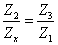 式中Z是阻抗(包括电阻、电容和电感),若交流信号的频率不太高,则电感和电容的影响可以忽略,此时 式中Z是阻抗(包括电阻、电容和电感),若交流信号的频率不太高,则电感和电容的影响可以忽略,此时 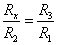 仍然成立。综合以上因素,交流信号的频率一般选择在1000Hz左右。 仍然成立。综合以上因素,交流信号的频率一般选择在1000Hz左右。
电导电极的选用应根据被测溶液电导率的大小而定,对电导率大的溶液,应选择电导池系数大的电极;反之,则选择电导池系数小的电极。
本实验的示零装置采用示波器,其灵敏度高而且很直观,但常受到外来电磁波的干扰,若采用低阻值的耳机则可避免这种干扰,但灵敏度不高,且克服不了测量过程中的人为因素。
应用电导法测量可以解决多种实际问题,它是电化学测量技术中最基本的方法之一,由于具有准确、快速的优点,所以在实际中得到广泛的应用,如水质的检验、电导滴定、通过测定电导确定工业用水的含盐量以及增大溶液的电导使电解时能耗降低等等。近年来,由于实验技术的不断发展,已出现许多测定电导率的专用仪器,它是把测出的电阻值换算成电导率直接显示在仪器上,其测量原理与惠斯登电桥类似。通过本实验学习希望同学们能够掌握这种方法,并学会运用电导知识分析电解质溶液的一些性能。25oC时醋酸解离平衡常数的文献值为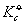 =1.754x10-5,同学们将计算结果与此比较,分析产生误差的原因,并对本实验装置的测量精度作出评价。 =1.754x10-5,同学们将计算结果与此比较,分析产生误差的原因,并对本实验装置的测量精度作出评价。
|