| ΓΓ ΒγΫβ÷ »ή“ΚΒΡΒΦΒγΡήΝΠ”…ΒγΒΦGά¥ΝΩΕ»Θ§Υϋ «ΒγΉηΒΡΒΙ ΐΘ§Φ¥ΘΚΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ ΒγΒΦΒΡΒΞΈΜ «ΓΑΈςΟ≈Ή”Γ±Θ§ΖϊΚ≈ΈΣΓΑSΓ±, ΓΓ ΫΪΒγΫβ÷ »ή“ΚΖ≈»κΝΫΤΫ––ΒγΦΪ÷°ΦδΘ§»τΝΫΒγΦΪΨύάκΈΣlΘ§ΒγΦΪΟφΜΐΈΣAΘ§‘ρ»ή“ΚΒΡΒγΒΦΈΣΘΚ ΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ Ϋ÷– ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ‘ρΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ Ά®≥ΘΫΪ“ΜΗωΒγΒΦ¬ “―÷ΣΒΡΒγΫβ÷ »ή“ΚΉΔ»κΒγΒΦ≥Ί÷–Θ§≤βΤδΒγΒΦΘ§ΗυΨί…œ ΫΦ¥Ω…«σ≥ωKcellΓΘ ΓΓ ‘Ύ―–ΨΩΒγΫβ÷ »ή“ΚΒΡΒΦΒγΡήΝΠ ±Θ§Ψ≠≥Θ Ι”ΟΡΠΕϊΒγΒΦ¬ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ Ϋ÷–cΈΣΒγΫβ÷ »ή“ΚΒΡ≈®Ε»Θ§ ΓΓ Ε‘”Ύ»θΒγΫβ÷ Θ®άΐ»γ¥ΉΥαΘ©ά¥ΥΒΘ§”…”ΎΤδΒγΒΦ¬ Κή–ΓΘ§Υυ“‘≤βΒΟΒΡ»ή“ΚΒΡΒγΒΦ¬ ”ΠΑϋά®Υ°ΒΡΒγΒΦ¬ Θ§Φ¥ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ ΒγΫβ÷ »ή“Κ «”…’ΐΓΔΗΚάκΉ”ΒΡ«®“Τά¥¥ΪΒίΒγΝςΒΡΘ§‘Ύ»θΒγΫβ÷ »ή“Κ÷–Θ§÷Μ”–Ϋβάκ≤ΩΖ÷ΒΡάκΉ”≤≈Ε‘ΒγΒΦ”–Ι±œΉΘ§Εχ‘ΎΈόœόœΓ ΆΒΡ»ή“Κ÷–Θ§ΒγΫβ÷ »Ϊ≤ΩΫβάκΘ§ΤδΡΠΕϊΒγΒΦ¬ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ Ϋ÷–ΠΆ+Θ§ΠΆ-Ζ÷±πΈΣ’ΐΓΔΗΚάκΉ”ΒΡΜ·―ßΦΤΝΩ ΐΘ§ ΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓ Ϋ÷–ΠΝΈΣ»θΒγΫβ÷ ΒΡΫβάκΕ»ΓΘ ΓΓ ¥ΉΥα‘ΎΥ°»ή“Κ÷–”–œ¬Ν–ΤΫΚβΘΚΓΓ ΓΓ ΤδΫβάκΤΫΚβ≥Θ ΐΈΣ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΫΪ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ¥Υ Ϋ≥ΤΈΣΑ¬ΥΙΧΊΆΏΕϊΒ¬Θ®OstwaldΘ©œΓ ΆΕ®¬…ΓΘΗΡ–¥≥…œΏ–‘ΖΫ≥ΧΈΣΘΚ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ “‘ ΓΓΓΓΓΓΓΓ 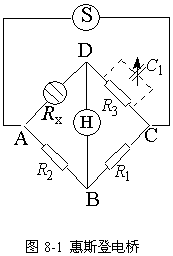 ΓΓΓΓ ’ϊάμΩ…ΒΟΘΚ ΓΓΓΓΓΓΓΓ ΓΓΒγΫβ÷ »ή“ΚΒΡΒγΒΦΆ®≥Θάϊ”ΟΜίΥΙΒ«Θ®WheatstonΘ©Βγ«≈≤βΝΩΘ§ΒΪ≤βΝΩ ±≤ΜΡή”Ο÷±ΝςΒγ‘¥Θ§“ρ÷±ΝςΒγΝςΆ®Ιΐ»ή“Κ ±Θ§ΒΦ÷¬ΒγΜ·―ßΖ¥”ΠΖΔ…ζΘ§≤ΜΒΪ ΙΒγΦΪΗΫΫϋ»ή“ΚΒΡ≈®Ε»ΗΡ±δ“ΐΤπ≈®≤νΦΪΜ·Θ§ΜΙΜαΗΡ±δΝΫΦΪΒΡ±Ψ÷ ΓΘ“ρ¥Υ±Ί–κ≤…”ΟΫœΗΏΤΒ¬ ΒΡΫΜΝςΒγΘ§ΤδΤΒ¬ Ά®≥Θ―ΓΈΣ1000HzΓΘΝμΆβΘ§ΙΙ≥…ΒγΒΦ≥ΊΒΡΝΫΦΪ≤…”ΟΕη–‘≤§ΒγΦΪΘ§“‘ΟβΒγΦΪ”κ»ή“ΚΦδΖΔ…ζΜ·―ßΖ¥”ΠΓΘ ΓΓ ΜίΥΙΒ«Βγ«≈ΒΡœΏ¬Ζ»γΆΦ8-1Υυ ΨΘ§Τδ÷–SΈΣΫΜΝς–≈Κ≈ΖΔ…ζΤςΘ§ R1ΓΔR2ΚΆR3 «»ΐΗωΩ…±δΫΜΝς±δΉηœδΒΡΉη÷ΒΘ§RxΈΣ¥ΐ≤β»ή“ΚΒΡΉη÷ΒΘ§HΈΣΕζΜζΘ®Μρ Ψ≤®ΤςΘ©Θ§C1ΈΣ‘ΎR3…œ≤ΔΝΣΒΡΩ…±δΒγ»ίΤςΘ§“‘ Βœ÷»ίΩΙΤΫΚβΓΘ≤βΕ® ±Θ§ΒςΫΎR1ΓΔR2ΓΔR3ΚΆC1Θ§ ΙH÷–ΈόΒγΝςΆ®ΙΐΘ§¥Υ ±Βγ«≈¥οΒΫΝΥΤΫΚβΓΘ‘ρ”–ΘΚ ΓΓΓΓ ΓΓRxΒΡΒΙ ΐΦ¥ΈΣ»ή“ΚΒΡΒγΒΦΘ§Φ¥ ΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ ”…”ΎΈ¬Ε»Ε‘»ή“ΚΒΡΒγΒΦ”–”ΑœλΘ§“ρ¥Υ Β―ι”Π‘ΎΚψΈ¬ΧθΦΰœ¬Ϋχ––ΓΘ ΓΓ ±Ψ Β―ιΆ®Ιΐ≤βΕ®0.02mol ΗυΨί |