|
1.实验前请认真阅读本实验的仪器“UJ-25型电位差计”的使用方法。
2.先用00号砂纸轻轻的把锌电极擦亮,蒸馏水洗净后,插入饱和Hg2(NO3)2溶液中3~5 s,使锌表面形成一层汞齐,取出后用镊子夹一小块滤纸轻擦电极,擦去表面灰色ZnO(用过的滤纸专门收集处理),然后用蒸馏水冲洗。将汞齐化的锌电极用滤纸擦干后,插入电极管并塞紧。将电极管上的虹吸管口浸入0.1000 mol・dm-3 ZnSO4溶液中,用吸耳球自支管抽气,使溶液吸入电极管内,并浸没电极,停止抽气,夹紧支管上的夹子,注意虹吸管内不能有气泡,也不能有漏液现象。接好电位差计测量电池电动势的线路,以饱和甘汞电极为正极,刚刚制得的锌电极为负极,测量电池:Zn|ZnSO4(0.1000 mol・dm-3)||KCl(饱和)|Hg2Cl2,Hg,Hg的电动势。利用饱和甘汞电极在该温度时的电极电势,计算出锌电极的电极电势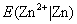 。 。
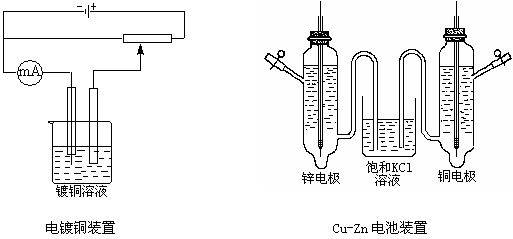
3.将铜电极在稀硝酸(6 mol・dm-3)溶液中浸洗后,用水冲洗,然后用蒸馏水淋洗。以此电极为阴极,另取一铜棒为阳极,在镀铜溶液内电镀,装置如图所示。电镀条件:电流密度为50 mA・cm-2左右,电镀时间20~30 min,待铜电极表面有一层致密的镀层后取出,依次用水、蒸馏水冲洗,插入电极管内,并在电极管内吸入浓度为0.1000 mol・dm-3的CuSO4溶液,即制得铜电极。以该电极为正极,饱和甘汞电极为负极,测量电池:Hg,Hg2Cl2|KCl(饱和)||CuSO4(0.1000 mol・dm-3)|Cu的电动势。根据该温度下饱和甘汞电极的电极电势,计算出铜电极的电极电势 。
4.将铜、锌电极按图连接好,测量电池:Zn|ZnSO4(0.1000mol・dm-3)|| CuSO4(0.1000mol・dm-3)|Cu的电动势。
5.25℃时,0.1000 mol・dm-3的CuSO4溶液的平均活度因子为0.16,0.1000 mol・dm-3的ZnSO4溶液的平均活度因子为0.15,由上面测得的铜电极和锌电极的电极电势计算铜电极和锌电极的标准电极电势。
|