知识点一:可逆电池热力学
一、可逆电池与不可逆电池
可逆电池是一个热力学的概念。电池中的过程以可逆方式进行时,电池为可逆电池。
可逆电池必须具有的两个条件:
(1)物质可逆;(2)能量可逆。
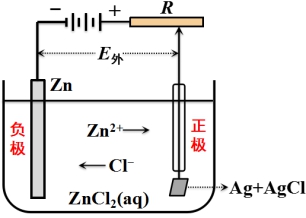
上图原电池表示为:
Pt, H2(p)|HCl(m)+AgCl(s)|Ag
(1)当![]() ,电池放电:
,电池放电:
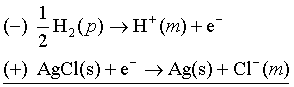
电池反应: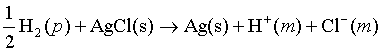
(2)![]() ,则对电池充电,成为电解池:
,则对电池充电,成为电解池:
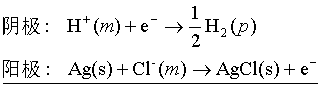
电解反应: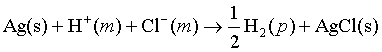
可见,上述电池的充、放电反应互为可逆反应,满足物质可逆,故有可能成为可逆电池。
【练习题】将Zn棒和Cu棒均插入到H2SO4溶液中,能否构成可逆电池?若Cu棒换成Zn棒呢?
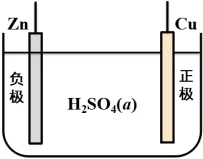
【提示:若![]() ,电池放电:
,电池放电:
(-)Zn极:![]()
(+)Cu极:![]()
若![]() ,对电池充电:
,对电池充电:
(阴)Zn极: ![]()
(阳)Cu极: ![]() ]
]
二、可逆电极的类型
1、第一类电极
(1)金属电极: ![]()
![]()
(2)汞齐电极: ![]()
![]()
(3)气体电极: ![]()
![]()
在碱性溶液中,氢电极![]() 可以认为分两步进行:
可以认为分两步进行:
![]()
![]()
总变化: ![]()
2、第二类电极
(1)金属——金属难溶盐电极。例如 甘汞电极和银一氯化银电极。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(2)金属——金属氧化物电极。例如
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
3、第三类电极
又称氧化还原电极。例如
![]() ,
,![]() :
: ![]()
![]() ,
,![]()
![]()
接下来让我们进行下一部分的学习
