(1)互变异构和酸性。α-碳上连有氢的1°和2°脂肪族硝基化合物能逐渐溶于强碱的水溶液生成盐类,表现出明显的酸性。一般认为这是由于这些硝基化合物中存在着下列互变异构平衡:
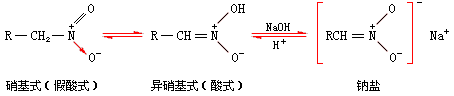
α-碳上的氢由于受到硝基-Ⅰ效应的影响,能够以质子的形式发生迁移。在无碱存在时,由于硝基式[nitro form,又叫假酸式(pseudoacid
form)]比异硝基式[isonitro form,又叫酸式(acid form)]稳定,所以平衡几乎完全偏向左边。当遇到碱时,因碱与酸式作用使平衡受到破坏,故反应不断向右进行,直至完全成盐。这种互变平衡移动的速度较慢,所以这类硝基化合物与碱作用要有一定的时间。
3°脂肪族硝基化合物和芳香硝基化合物分子中无α-氢,不能发生这种互变异构,所以它们不溶于氢氧化钠溶液。
硝基化合物的这种性质可用于分离提纯具有α-氢的硝基化合物。
(2)还原反应。硝基化合物易被还原,在不同条件下还原得到不同的产物。
脂肪族硝基化合物在强还原条件下还原产物是1°胺:
![]()
若在中性条件下用金属作还原剂,则得N-烷基羟胺:
![]()
芳香族硝基化合物在酸性条件下还原,产物也是1°胺:
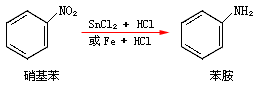
在中性条件下还原,主要生成N-羟基苯胺:

采用适当的催化剂进行催化氢化,也可将硝基苯一步还原生成对氨基苯酚:
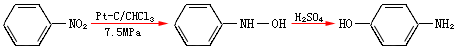
若在碱性条件下还原,则生成偶氮化合物:
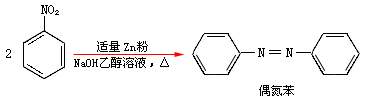
偶氮苯实际上是由N-羟基苯胺互相缩合而成的。
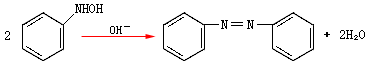
(3)与亚硝酸的反应。1°、2°硝基化合物可与亚硝酸发生反应。1°硝基化合物与亚硝酸作用,生成蓝色的α-亚硝基衍生物,溶于碱则生成红色:
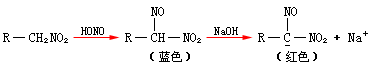
2°硝基化合物与亚硝酸作用,生成蓝色的亚硝基衍生物,因该衍生物无α-氢原子,所以不溶于碱:
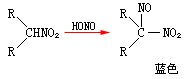
3°硝基化合物不能与亚硝酸反应。
此反应可用于区别三种不同的硝基化合物。
(4)硝基对苯环邻、对位上取代基的影响。在苯环上和硝基处于邻、对位的某些取代基,常显示出一些特殊的活泼性,这主要是因为它们受到了硝基强吸电子效应的影响。与硝基处于间位的基团受这种电子效应的影响较小。现分述如下:
①增强卤原子活泼性。苯环上的卤素原子很不活泼,若在卤原子的邻、对位逐步引入硝基,则卤原子的活泼性逐渐增强。例如:
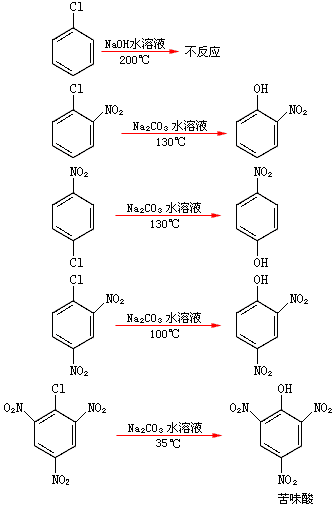
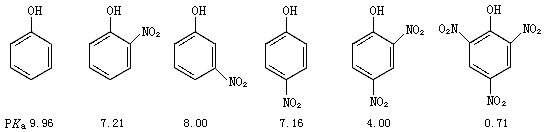
②增强酚羟基的酸性。在邻、对位上的硝基能使酚羟基的酸性增强,处于间位的硝基也能增加酚羟基的酸性,但效果不及邻、对位上的硝基显著。芳环上引入硝基越多,酚的酸性越强。例如: